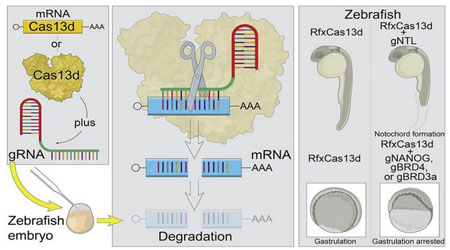
El profesor de la Universidad Pablo de Olavide, Miguel Ángel Moreno Mateos, investigador Ramón y Cajal en el Centro Andaluz de Biología del Desarrollo (CABD), co-lidera junto al investigador del Stowers Institute de EE.UU. Ariel Bazzini, un estudio basado en el empleo de la tecnología CRISPR-Cas para entender el papel que juega el ARN materno, depositado en el oocito, en las primeras horas del desarrollo. La investigación ‘CRISPR-Cas13d Induces Efficient mRNA Knockdown in Animal Embryos’ ha sido portada en la prestigiosa revista internacional Developmental Cell, publicada ayer lunes 28 de septiembre.
Este sistema fue primero implementado en sistemas ex vivo en cultivos de células de mamífero, y ahora en este trabajo ha sido optimizado por Miguel A. Moreno Mateos y su equipo en distintos modelos animales como el pez cebra o en ratones. “La tecnología que hemos implementado puede ser la base de muchas aproximaciones científicas y de muchas aplicaciones en biología y biomedicina”, afirma el investigador de la UPO, que destaca este trabajo no solo por la nueva herramienta que han perfeccionado si no por su futuro desarrollo tecnológico. Así, por ejemplo, esta herramienta se puede modificar para que, en lugar de cortar el ARN, Cas13 lo modifique o los investigadores sean capaces de localizarlo dentro de la célula, aproximaciones que ya han sido demostradas en sistemas ex vivo pero no en modelos animales.
En el trascurso de la investigación, Miguel Ángel Moreno Mateos destaca que no todos los sistemas CRISPR-Cas13 que funcionaban adecuadamente en células en cultivo después lo hicieron in vitro. “Al principio fue un poco desesperante porque probamos varias proteínas Cas13, como LwaCas13a, PspCas13b y PguCas13b, y ninguna parecía funcionar adecuadamente in vivo. Solo RfxCas13d demostró una buena eficiencia y especificidad” comenta el investigador. Por su parte, Ariel Bazzini, co-lider de este trabajo, afirma que “aunque existían tecnologías anteriores para eliminar o inhibir la función del RNA en animales, CRISPR-Cas13d es más eficiente y fiable, además de más económica que las que existen actualmente”.
Comprender cómo se inicia la vida
El trabajo parte de un objetivo claro, que es conocer qué factores maternos depositados en el oocito en forma de ARN mensajero, que dará lugar a proteínas, tienen un papel crucial en los primeros pasos de la vida. Esta herramienta es la base para estudiar, de manera sistemática, estos factores maternos y su papel durante el desarrollo temprano animal.
Miguel A. Moreno Mateos, investigador del CABD.
Y es que el laboratorio de Miguel Ángel Moreno combina el desarrollo de tecnología CRISPR-Cas in vivo con líneas de biología fundamental de desarrollo temprano. “Tratamos de entender cómo se inicia la vida, estudiar las funciones genéticas maternas y comprender cómo dichos factores maternos impulsan las primeras etapas de desarrollo”, explica el investigador, quien añade que “comprendiendo cómo arranca el desarrollo de un animal podemos entender mejor los mecanismos de la reprogramación celular que tanto impacto tiene hoy por hoy en biomedicina”. Así, esta herramienta podría contribuir, por ejemplo, al estudio de la infertilidad, la medicina regenerativa y los problemas de desarrollo en general.
Además, los resultados demuestran que la técnica se puede aplicar a una amplia gama de modelos acuáticos y terrestres, incluidos embriones de pez cebra, medaka, killifish y ratones.
El equipo del investigador Miguel Ángel Moreno es pionero en la optimización de la tecnología CRISPR-Cas13. De hecho, el estudio publicado en Developmental Cell es la base en la que se sustenta la primera fase de un proyecto de investigación financiado por el Consejo Superior de Investigaciones Científicas cuyo objetivo es destruir el genoma del coronavirus SARS–CoV-2 empleando la herramienta de edición genética de última generación CRISPR–Cas13d.
Referencia bibliográfica: Kushawah Gopal, Hernandez-Huertas Luis et al.CRISPR-Cas13d Induces Efficient mRNA Knockdown in Animal Embryos. Developmental Cell. (2020)