En este informe se revisan los tiempos para que un Organismo Notificado pueda dar el certificado según MDD o MDR para un producto sanitario de los precisos para la COVID.
Los tiempos medios son los siguientes:
– tiempo para iniciar el procedimiento: menos de 15 para MDD y menos de 30 dias para MDR
– tiempo para completar el procedimiento:
– para un cliente actual 1 a 3 meses y para nuevas categorías 3 a 6 meses
– para un nuevo cliente y productos clase IIa de 1 a 6 meses y para clase IIb de 6 a 12 meses (p.ej. ventiladores pulmonares)
– para productos IVDD los tiempos van entre 1 y 3 meses. Para IVDR que pueden ser de la clase D indican que el procedimiento de evaluación no puede aun completarse. En este informe se revisan los tiempos asociados para la aprobación de productos que esta claro que no son adecuados para poder ser usados en la pandemia, por ello las Autoridades Sanitarias como las españolas tuvieron que usar la ruta de la investigación clínica para poder realizar la evaluación de conformidad

El equipo de investigadores observó cambios en el...
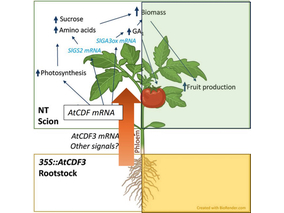
El gen AtCDF3 promueve una mayor producción de az...
Un estudio con datos de los últimos 35 años, ind...
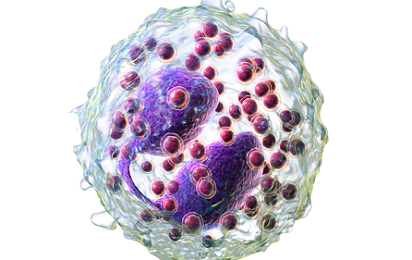
En nuestro post hablamos sobre este interesante tipo de célula del si...
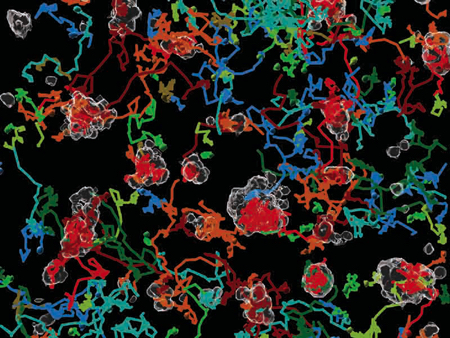
La revista ‘Nature Protocols’ selecciona esta técnica como “pro...
Portal de biotecnología en España
¡Suscríbase a nuestro newsletter para estar al día con las últimas noticias y ofertas!
2013 © Biotech-Spain.com - Site Developments SL. Todos los derechos reservados. Terminos y Condiciones | Política de Privacidad
Articles
Directory
