La pasada semana la EMA hizo pública la fecha definitiva para la implementación y “go live” de la nueva versión de Eudravigilance.
Este cambio supone la obligatoriedad para los Titulares de Autorización de Comercialización, de adaptar sus sistemas de gestión de casos en farmacovigilancia de ICH E2B(R2)/M2 a ISO/ICH E2B(R3).
Una base de datos que cumpla con las normativas internacionales y permita la comunicación directa con partners y Autoridades (Gateway) se convierte en una herramienta imprescindible para cualquier departamento de Farmacovigilancia.
La correcta gestión de los datos no solo garantiza tranquilidad frente auditorías e inspecciones en Farmacovigilancia, sino que sirve como una herramienta de optimización de recursos y procedimientos, permitiendo la evaluación global de la seguridad de nuestros medicamentos de una forma sencilla y eficiente.
En Azierta somos expertos en Farmacovigilancia y conocemos la importancia y responsabilidad de gestionar una unidad de Farmacovigilancia.
Además contamos con un innovador softwate para la gestion de la Farmacovigilancia (Vigilazierta) que integra todas las funcionalidades que necesitas para simplificar tus procesos, de acuerdo con la normativa vigente.
Si quieres conocernos mejor, o ampliar información no dudes en visitarnos en nuestra web de VIgilazierta.
Fuente: Nota informativa de la EMA (Green light given for new EudraVigilance system for collection and monitoring of suspected adverse reactions)

La mejor actitud que podemos adoptar es la de trat...

El equipo de investigadores observó cambios en el...
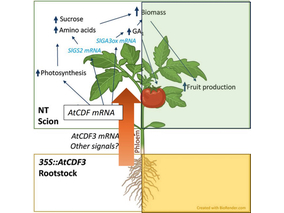
El gen AtCDF3 promueve una mayor producción de az...
En nuestro post hablamos sobre este interesante tipo de célula del si...

Los resultados muestran que el adenocarcinoma presenta una angiogénes...
Portal de biotecnología en España
¡Suscríbase a nuestro newsletter para estar al día con las últimas noticias y ofertas!
2013 © Biotech-Spain.com - Site Developments SL. Todos los derechos reservados. Terminos y Condiciones | Política de Privacidad
Articles
Directory